La espectrometría de absorción atómica (AAS) es una técnica analítica de referencia para la determinación cuantitativa de elementos metálicos en una amplia variedad de muestras. Basada en la absorción de luz por átomos libres en el estado fundamental, permite medir concentraciones extremadamente bajas con notable precisión. Utilizada en campos tan diversos como la alimentación , el medio ambiente , la industria farmacéutica y los materiales , la AAS desempeña un papel fundamental en el control de calidad, el cumplimiento normativo y la investigación científica. Este artículo explora los principios fundamentales de este método, su funcionamiento, sus principales aplicaciones y sus ventajas analíticas.
Tabla de contenido
Principio de la espectrometría de absorción atómica
Un método óptico basado en la absorción atómica
La espectrometría de absorción atómica es un método de análisis elemental basado en un fenómeno físico simple: la absorción de la radiación luminosa por los átomos en su estado fundamental. A diferencia de otras técnicas espectroscópicas basadas en la emisión de luz, la espectrometría de absorción atómica (EAA) mide la cantidad de luz absorbida por un átomo dado al exponerse a una fuente de radiación electromagnética monocromática, emitida a la longitud de onda característica del elemento analizado.
Cuando un haz de luz atraviesa una nube de átomos vaporizados, parte de esta radiación se absorbe si su longitud de onda corresponde a la energía necesaria para excitar los electrones en estos átomos. Esta pérdida de intensidad luminosa, medida antes del paso de (I₀) y después del paso de (Iₜ) a través del medio atómico, está directamente relacionada con la concentración del elemento objetivo en la muestra.
La ley de Beer-Lambert en el corazón de la cuantificación
La relación matemática entre absorbancia y concentración se basa en la ley de Beer-Lambert, formulada de la siguiente manera:
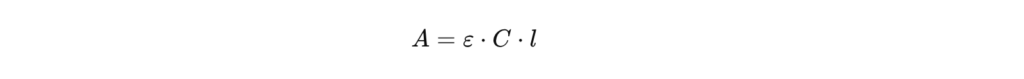
O :
- A es la absorbancia,
- ε es el coeficiente de extinción molar,
- l es la longitud del tanque,
- Es la concentración de la solución.
Esta ley lineal se aplica dentro de un rango de concentración bien definido. Cuando la concentración es demasiado alta o existen interferencias, pueden aparecer desviaciones de la linealidad, lo que requiere correcciones instrumentales o la dilución de la muestra.
De Kirchhoff al SAA moderno: una evolución tecnológica continua
El concepto de absorción atómica se remonta a los experimentos fundamentales de Gustav Kirchhoff en el siglo XIX. Kirchhoff demostró que las líneas oscuras observadas en un espectro de absorción coincidían con las líneas brillantes en el espectro de emisión de elementos calentados en una llama. Estas observaciones sentaron las bases de la espectroscopia atómica moderna.
La verdadera revolución en la AAS se produjo en la década de 1950 gracias al trabajo del físico australiano Alan Walsh, quien introdujo el principio de absorción atómica utilizando fuentes de luz específicas para cada elemento. Este enfoque permitió un análisis más preciso y reproducible, en particular para elementos metálicos.
Desde entonces, la AAS ha experimentado numerosas mejoras tecnológicas: fuentes de luz más estables, sistemas de corrección de fondo (como el efecto Zeeman), dispositivos de atomización optimizados (llama, horno de grafito, generador de hidruro), automatización de análisis e integración de software de procesamiento de datos. Estos avances han ampliado el alcance de las aplicaciones de la AAS, a la vez que han aumentado la sensibilidad, la fiabilidad y la productividad de esta técnica.
Hoy en día, la espectrometría de absorción atómica se considera un método de referencia para la determinación de metales traza, gracias a su robustez, especificidad y su capacidad de proporcionar resultados cuantitativos reproducibles en una amplia variedad de matrices.
Equipos utilizados en espectrometría de absorción atómica
Composición de un espectrómetro de absorción atómica
Un espectrómetro de absorción atómica generalmente consta de seis elementos principales, dispuestos en serie a lo largo del camino óptico:
- Una fuente de luz que emite radiación monocromática en la longitud de onda específica del elemento en estudio.
- Un modulador , mecánico o electrónico, que permite distinguir la luz de análisis del ruido de fondo.
- Un atomizador , encargado de transformar la muestra en una nube de átomos libres en el estado fundamental.
- Un monocromador que aísla la línea de interés eliminando las longitudes de onda parásitas.
- Un detector , generalmente un fotomultiplicador, que mide la intensidad de la luz residual.
- Un sistema de procesamiento de datos , que convierte la señal luminosa en absorbancia y luego en concentración.
espectrómetros de haz único y de haz doble . En la versión de haz único, la radiación pasa sucesivamente por el atomizador y luego por el monocromador antes de llegar al detector. En la versión de haz doble, un divisor óptico divide el haz en dos trayectorias: una pasa por el atomizador (haz de análisis) y la otra lo desvía (haz de referencia). Las dos señales se comparan para corregir las fluctuaciones de la fuente y mejorar la estabilidad de la medición.
Las diferentes fuentes de luz utilizadas
La calidad de la fuente de luz determina la selectividad y la sensibilidad de la medición. En la espectrometría de absorción atómica, se utilizan principalmente lámparas que emiten líneas espectrales estrechas específicas para cada elemento.
lámpara de cátodo hueco (HCL) la . Contiene un cátodo del metal a analizar, un ánodo de tungsteno y un gas inerte (argón o neón) a baja presión. Una descarga eléctrica entre los electrodos excita los átomos del cátodo, emitiendo un espectro de líneas características al volver al estado fundamental.
La lámpara de vapor metálico se basa en el mismo principio, pero contiene el elemento directamente en forma metálica. Es adecuada para metales fácilmente volátiles como el sodio o el mercurio.
Finalmente, las lámparas de descarga sin electrodos (EDL) se utilizan para elementos volátiles difíciles de analizar con una lámpara de cátodo hueco (arsénico, antimonio, selenio, bismuto). Ofrecen mayor intensidad y una mayor vida útil.
El modulador: gestión de la señal de análisis
El modulador permite interrumpir periódicamente el haz de luz incidente para distinguir la señal útil (luz absorbida por el analito) del ruido de fondo (luz parásita o emisiones de llama). Se utilizan habitualmente dos tipos de modulación:
- Modulación mecánica mediante un cortador óptico, a menudo un disco giratorio que bloquea y libera cíclicamente el haz.
- Modulación eléctrica mediante la alimentación de corriente alterna de la lámpara. En este caso, la corriente alterna genera una señal periódica más fácil de aislar y amplificar. Este método también facilita la discriminación entre los fotones absorbidos por la muestra y los emitidos por la fuente.
El monocromador: selección de la línea de interés
La función del monocromador es filtrar la radiación transmitida por el atomizador para retener únicamente la longitud de onda específica del elemento analizado. De esta manera, se eliminan las líneas del gas de llenado, las líneas secundarias y las emisiones parásitas de la llama o del horno.
Consta de una rendija de entrada, un sistema dispersivo (prisma o red de difracción) y una rendija de salida. La red descompone el haz de luz en un espectro de longitudes de onda, y la rotación del dispositivo permite seleccionar con precisión la línea de análisis.
El ancho de banda espectral (normalmente entre 0,2 y 2 nm) debe elegirse para garantizar una buena separación de las líneas manteniendo una intensidad suficiente.
El detector: conversión de la señal luminosa
El detector más utilizado en AAS es el tubo fotomultiplicador . Este transforma la señal luminosa transmitida por el monocromador en una señal eléctrica proporcional a la intensidad luminosa recibida. Esta señal se amplifica, se convierte y se procesa digitalmente.
En algunos instrumentos recientes, también encontramos fotodiodos o matrices de diodos , capaces de medir varias longitudes de onda simultáneamente. Sin embargo, estos dispositivos son menos comunes en la AAS clásica, que sigue siendo un método de un solo elemento.
Técnicas de atomización: llama, horno de grafito, hidruros, vapor frío
Atomización por llama: el método más extendido
El método más antiguo y comúnmente utilizado es la atomización por llama , también llamada AAS por llama . Se basa en pulverizar la solución a analizar en forma de un aerosol muy fino, que posteriormente se introduce en una llama producida a partir de una mezcla de combustible y oxidante.
Las llamas más utilizadas son:
- Aire/acetileno : temperatura alrededor de 2300 a 2500 °C
- Óxido nitroso/acetileno : hasta 2900 °C, utilizado para elementos refractarios
Hay dos tipos de quemadores:
- El quemador de llama laminar (premezclado), que garantiza una mejor estabilidad de la llama y, por tanto, una mayor reproducibilidad de las mediciones.
- El de llama turbulenta (difusión), utilizado en contextos específicos donde la seguridad del gas es un problema.
En esta configuración, el nebulizador transforma la solución líquida en una niebla de aerosol, de la cual solo una pequeña fracción alcanza la llama. Las gotas se secan y luego se descomponen térmicamente, liberando gradualmente los átomos del elemento a analizar.
Esta técnica es rápida, robusta y suficiente para elementos presentes en concentraciones superiores a µg/L. Sin embargo, presenta limitaciones debido a su sensibilidad y a que la atomización es continua, lo que resulta en una pérdida significativa de muestra.
Atomización electrotérmica: el horno de grafito
Para análisis de concentraciones muy bajas, el AAS electrotérmico (o AAS en horno de grafito). Este método se basa en un tubo de grafito en el que se deposita una pequeña cantidad de muestra (de 5 a 100 µL) mediante un microinyector.
El tubo se calienta por efecto Joule según un programa térmico de tres etapas :
- Secado : eliminación del disolvente a baja temperatura (alrededor de 100 °C)
- Descomposición o pirólisis : evaporación de compuestos orgánicos e impurezas sin atomización del elemento objetivo.
- Atomización : liberación de átomos a alta temperatura (hasta 3000°C), en atmósfera inerte (argón).
El horno permite mantener temporalmente los vapores atómicos en un volumen confinado, aumentando así la probabilidad de interacción con el haz de luz y por tanto la sensibilidad de la medición.
Este método es adecuado para elementos presentes en cantidades traza, pero requiere un control riguroso de las temperaturas y del programa térmico, ya que de lo contrario pueden producirse pérdidas analíticas o la formación de interferencias.
Atomización por generación de hidruros: una solución para ciertos elementos volátiles
Ciertos elementos como el arsénico (As), el selenio (Se), el antimonio (Sb), el bismuto (Bi) o el plomo (Pb) forman compuestos volátiles llamados hidruros . En estos casos, la atomización puede mejorarse mediante un paso previo de generación de hidruros volátiles.
El principio se basa en una reacción química entre el analito (en solución ácida) y un agente reductor , como el borohidruro de sodio (NaBH₄) . Esta reacción forma hidruros gaseosos, que posteriormente son transportados por un gas inerte a una celda de atomización calentada , donde los hidruros se descomponen térmicamente para liberar los átomos.
Esta técnica ofrece una excelente sensibilidad y una selectividad muy buena, especialmente para elementos que forman hidruros fácilmente. Sin embargo, requiere un sistema específico de generación de hidruros, que suele instalarse antes del espectrómetro.
¿Estas buscando un análisis?

Nebulización y preparación de muestras
El papel central del nebulizador
El nebulizador es un componente esencial del sistema de atomización, especialmente en modo llama. Su función es transformar la solución líquida que contiene el analito en un aerosol muy fino compuesto de microgotas. Esta niebla se transporta posteriormente a la llama, donde se llevan a cabo correctamente los pasos de secado, descomposición y atomización.
Una nebulización eficaz debe producir gotas lo más pequeñas y homogéneas posible. De hecho, solo las microgotas que llegan a la llama tienen probabilidades de atomizarse correctamente. Las gotas demasiado grandes son eliminadas por las paredes del sistema o arrastradas por el drenaje. Se estima que entre el 5 % y el 10 % del volumen nebulizado llega a la zona de atomización, lo que hace esencial la optimización del proceso.
Tipos de nebulizadores
En la espectrometría de absorción atómica se utilizan dos familias principales de nebulizadores.
El nebulizador neumático es el más común. Funciona según el principio de aspirar la solución mediante un chorro de gas (generalmente aire o argón) que crea vacío a la salida de un capilar. El líquido se proyecta a alta velocidad y se fragmenta en finas gotas. Los sistemas de clasificación por impacto o hélice eliminan las partículas más grandes antes de que entren en la llama.
El nebulizador ultrasónico , mucho más raro en AAS, se basa en la vibración de un cristal de cuarzo sobre el que fluye la solución. Las ondas ultrasónicas fragmentan la superficie del líquido en un aerosol. Este tipo de nebulizador tiene mayor eficiencia, pero es más caro y frágil.
La elección del nebulizador depende de la viscosidad de la solución, el caudal requerido, la naturaleza de la matriz y los requisitos de sensibilidad.
Preparación de muestras: soportes y precauciones
Para garantizar la calidad del análisis, la muestra debe prepararse en condiciones controladas. Generalmente se mineraliza con ácidos fuertes (nítrico, perclórico, sulfúrico) para disolver los elementos metálicos presentes en forma iónica o combinada. Este paso también simplifica la matriz y limita las interferencias químicas.
Las soluciones obtenidas se filtran y se transfieren a frascos limpios, inertes y herméticos , generalmente de polipropileno o vidrio de borosilicato. Estos recipientes deben ser compatibles con los metales a analizar para evitar la contaminación o adsorción de los analitos en las paredes.
A continuación se presentan algunas buenas prácticas a seguir:
- Utilice únicamente recipientes destinados al análisis de metales.
- Compruebe la compatibilidad química del material con soluciones ácidas.
- Evite el contacto prolongado con el aire para limitar la oxidación.
- Prepare soluciones madre y estándares en el mismo tipo de matriz que la muestra.
El volumen de inyección también es un parámetro crítico. En el modo de llama, la muestra se aspira continuamente durante todo el análisis. Sin embargo, en el modo de horno de grafito, el volumen debe medirse con precisión (a menudo entre 10 y 50 µL) y depositarse en el centro del tubo mediante un microinyector. El uso de sistemas de inyección automatizados garantiza una mejor reproducibilidad y trazabilidad de los ensayos.
También se debe prestar especial atención a los blancos analíticos y las soluciones de calibración . El blanco se utiliza para comprobar la ausencia de contaminación del reactivo o los recipientes. Los estándares, por otro lado, son esenciales para establecer la curva de calibración utilizada en el cálculo de las concentraciones.
Interferencias analíticas y limitaciones del método
Interferencias químicas
Las interferencias químicas se producen cuando los componentes de la matriz forman compuestos estables o poco volátiles con el elemento analizado. Esto puede reducir la eficiencia de la atomización y provocar una subestimación de la concentración real.
Por ejemplo, en matrices que contienen fósforo, el calcio puede formar fosfato de calcio, difícil de atomizar. De igual manera, ciertos aniones, como los sulfatos o carbonatos, pueden precipitar metales pesados en forma de sales insolubles.
Para limitar estos efectos, son posibles varias estrategias:
- Añadir modificadores químicos (agentes complejantes, agentes enmascaradores) que impidan la formación de compuestos estables.
- Trabajar a temperaturas de atomización más altas (especialmente en hornos de grafito).
- Optimizar la composición de la llama (llama rica o pobre) según las reacciones esperadas.
Interferencia espectral
Las interferencias espectrales corresponden a absorbancias parásitas generadas por especies distintas del analito, pero que absorben en longitudes de onda cercanas. Estas interferencias también pueden resultar de la dispersión de la luz por partículas sólidas o de la luminiscencia emitida por la llama o la matriz.
Son particularmente problemáticos cuando la línea de absorción del elemento está próxima a la de otros componentes presentes en la muestra, o en casos de fuertes emisiones parásitas (llama caliente, elementos fácilmente excitables).
Para corregirlos se implementan varias soluciones:
- Utilizando un monocromador de alta resolución con un ancho de banda estrecho.
- Configuración de un sistema de corrección de fondo , utilizando una lámpara de deuterio o el efecto Zeeman.
- Elección de una longitud de onda alternativa , si existe para el elemento objetivo.
Efectos de matriz
Los efectos de matriz incluyen todas las perturbaciones relacionadas con las propiedades físicas de la muestra: viscosidad, tensión superficial, presión osmótica y conductividad. Estos parámetros influyen en la nebulización, la dispersión en la llama y la distribución de átomos en el volumen de absorción.
Una muestra con una alta concentración de sal, por ejemplo, puede provocar una cristalización rápida durante la nebulización o la formación de depósitos en el nebulizador, alterando la estabilidad de la señal. Las matrices biológicas ricas en proteínas o lípidos pueden interactuar con el tubo de grafito y distorsionar los ciclos de atomización.
Para limitar los efectos de la matriz, se recomienda:
- Realizar una dilución adecuada de las muestras sin bajar del LOQ.
- Utilice el método de adición estándar , que implica agregar una cantidad conocida de analito a la muestra para compensar los efectos de la matriz.
- Utilice modificadores de matriz , como sales de aluminio o paladio, que estabilizan el analito en el tubo de grafito.
Limitaciones técnicas y analíticas
A pesar de sus muchas ventajas, la espectrometría de absorción atómica tiene ciertas limitaciones intrínsecas:
- Método de un solo elemento : Cada análisis requiere una lámpara específica y una calibración específica para el elemento. No es posible analizar varios elementos simultáneamente, salvo por alternancia.
- Rango dinámico reducido : La absorbancia sigue una relación lineal dentro de un área restringida. Más allá de este rango, la respuesta se vuelve no lineal, lo que genera resultados inexactos.
- Tiempo de análisis : Aunque rápido en modo llama, el método se vuelve más lento en horno de grafito o generación de hidruro, debido a los ciclos de calentamiento e inyecciones sucesivas.
- Costo y mantenimiento : Reemplazar lámparas, mantener el nebulizador y los sistemas de inyección automáticos pueden generar costos importantes a largo plazo.
A pesar de estas limitaciones, la AAS sigue siendo una de las técnicas más robustas y mejor documentadas para la determinación de oligoelementos. El uso combinado de dispositivos de corrección, métodos de preparación adecuados y buenas prácticas de laboratorio permite minimizar el impacto de las interferencias y aprovechar al máximo el potencial analítico de este método.

Áreas de aplicación de la espectrometría de absorción atómica
Monitoreo ambiental y análisis regulatorio
La espectrometría de absorción atómica se utiliza ampliamente en el campo ambiental , particularmente para monitorear la calidad del agua , el suelo , los lodos y los efluentes industriales .
Puede detectar metales tóxicos como plomo, cadmio, arsénico, mercurio y cromo hexavalente en concentraciones muy bajas, a menudo inferiores a 1 µg/L. Estos análisis se rigen por normas internacionales como la Directiva Marco del Agua (2000/60/CE) norma NF EN ISO 5961 para la determinación de cadmio.
En laboratorios acreditados, el SAA se utiliza para:
- Control del agua potable, aguas superficiales y aguas subterráneas
- Análisis de lixiviados de residuos
- Caracterización de suelos y sedimentos contaminados
Seguridad alimentaria y nutracéutica
En las alimentaria y nutracéutica , la SAA se utiliza para verificar la conformidad de los productos con los límites máximos de residuos de metales pesados establecidos por la normativa europea.
Se utiliza para medir elementos no deseados en:
- Materias primas agrícolas (verduras, cereales, hierbas)
- Productos procesados (jugos, suplementos alimenticios, polvos nutricionales)
- Envases de alimentos en relación con las pruebas de migración
Estos análisis permiten evaluar la seguridad sanitaria de los productos alimenticios, garantizar el cumplimiento de la normativa (reglamento CE 1881/2006) y validar las declaraciones nutricionales sobre el contenido en minerales (hierro, zinc, magnesio, calcio, etc.).
Cosméticos y productos de cuidado personal
En la cosmética , la espectrometría de absorción atómica se utiliza para detectar la presencia de contaminantes metálicos en los ingredientes o productos terminados.
Los metales indeseables más vigilados son el níquel (Ni) , el plomo (Pb) , el cadmio (Cd) , el mercurio (Hg) y el arsénico (As) , debido a su potencial tóxico y alergénico. Estas sustancias no deben estar presentes en los cosméticos terminados, salvo en trazas técnicamente inevitables.
Los laboratorios también analizan:
- Pigmentos y colorantes (óxidos de hierro, dióxido de titanio, etc.)
- Protectores solares y humectantes
- Productos para el cabello o maquillaje
La SAA garantiza así la seguridad de uso y el cumplimiento de la normativa cosmética (CE 1223/2009) .
Salud animal y farmacia
En salud animal , la SAA se utiliza para evaluar el contenido mineral de los alimentos para animales y para detectar una posible contaminación por metales pesados en las formulaciones veterinarias.
sector farmacéutico , la espectrometría de absorción atómica permite controlar la pureza de excipientes e ingredientes activos según los requisitos de la directiva ICH Q3D sobre impurezas elementales. Esta directiva impone umbrales estrictos para los elementos clasificados según su toxicidad (grupos 1 a 3) y exige una rigurosa validación de los métodos analíticos.
Las aplicaciones incluyen:
- Control de sales minerales (Ca, Fe, Mg, Zn, etc.) en soluciones inyectables
- La determinación de plomo, arsénico, mercurio y cadmio en ingredientes farmacéuticos
- Verificación de insumos de procesos catalíticos (platino, paladio)
Control de materiales y procesos industriales
El SAA también se utiliza en las industrias metalúrgica , química de materiales . Garantiza el control de calidad de las materias primas y los productos terminados.
Los análisis pueden referirse a:
- Aleaciones metálicas ( aluminio, acero, latón) para comprobar su composición.
- Soluciones para el tratamiento de superficies ( baños galvánicos, decapantes)
- Materiales en contacto con alimentos , para probar migraciones específicas
Este método es especialmente útil en laboratorios de I+D y laboratorios de producción para garantizar el cumplimiento normativo (reglamento CE 1935/2004, FDA) , optimizar formulaciones o analizar defectos de fabricación.
Servicios de análisis de espectrometría de absorción atómica con YesWeLab
Una solución centralizada para todos sus análisis básicos
YesWeLab le brinda acceso a una gama completa de análisis de espectrometría de absorción atómica , ya sea para ensayos únicos, campañas de monitoreo ambiental o validaciones de cumplimiento normativo.
Gracias a una plataforma digital intuitiva , los fabricantes pueden:
- Busca y selecciona el análisis adaptado a tu producto o a tu problemática en el catálogo de YesWeLab
- Solicite el análisis en línea en solo unos clics
- Seguimiento de la entrega de muestras y del progreso de las pruebas
- Descargue los resultados directamente desde un espacio seguro
Esta operación simplificada ahorra tiempo valioso y garantiza una trazabilidad completa de las operaciones.
Servicios que cumplen con los más altos estándares
Los análisis que ofrece YesWeLab se realizan en laboratorios acreditados por la norma ISO 17025 y, para ciertos parámetros, en laboratorios reconocidos por COFRAC . Los métodos implementados cumplen con las normas vigentes:
- Normas NF EN ISO para agua, suelo, lodos y productos alimenticios
- ICH Q3D para impurezas elementales en productos farmacéuticos
- Reglamento (CE) 1881/2006 sobre metales en los alimentos
- Reglamento (CE) 1223/2009 para cosméticos
Los resultados se entregan con incertidumbre de medición controlada , controles de calidad integrados y comentarios técnicos si es necesario.



