L’acide acétique, aussi appelé acide éthanoïque, est un composé organique essentiel dans de nombreuses industries, notamment l’agroalimentaire, la chimie et la pharmacie. Connu pour être le principal constituant du vinaigre, il joue également un rôle fondamental dans la fabrication de nombreux produits industriels et pharmaceutiques. Ce liquide incolore, au goût et à l’odeur caractéristiques, est couramment utilisé comme solvant, réactif chimique et additif alimentaire. Cet article explore en détail les propriétés, la production et les applications de l’acide acétique, en mettant en avant son importance et les méthodes d’analyse en laboratoire.
YesWeLab vous offre une gamme complète de services d’analyses de laboratoire, alliant expertise et technologies de pointe pour garantir la qualité et la conformité de vos produits.
Table des matières
Qu'est-ce que l'acide acétique ?
Définition et formule chimique
Propriétés physico-chimiques
L’acide acétique est un acide carboxylique de formule chimique C₂H₄O₂, souvent représenté sous la forme développée CH₃COOH. Son groupe fonctionnel -COOH lui confère son acidité caractéristique. Il appartient à la famille des acides monocarboxyliques et se classe parmi les acides faibles en solution aqueuse. À ne pas confondre avec l’acide peracétique (C₂H₄O₃), un agent oxydant puissant utilisé comme désinfectant et stérilisant, dont les propriétés chimiques et applications diffèrent de celles de l’acide acétique.
L’acide acétique peut exister sous différentes formes :
- Acide acétique glacial : Forme pure à 99,5 %, qui se solidifie en dessous de 16,6 °C. Il est ainsi nommé en raison de son aspect cristallisé lorsqu’il gèle.
- Solutions aqueuses : Selon la concentration, il est utilisé comme régulateur d’acidité dans l’industrie agroalimentaire.
En milieu aqueux, l’acide acétique se dissocie partiellement en ion acétate (CH₃COO⁻) et ion hydronium (H₃O⁺), ce qui explique son acidité modérée avec un pKa de 4,76. Cette caractéristique le différencie des acides forts comme l’acide sulfurique ou l’acide chlorhydrique.
L’acide acétique possède des propriétés spécifiques qui expliquent son utilisation dans de nombreux domaines industriels et scientifiques.
- Température de fusion et d’ébullition :
- Température de fusion : 16,6 °C
- Température d’ébullition : 117,9 °C
- Densité : 1,05 g/cm³ à 20 °C
- Solubilité : Entièrement miscible avec l’eau, l’éthanol, l’éther diéthylique et d’autres solvants organiques.
- Acidité : pKa = 4,76, caractéristique d’un acide faible.
- Inflammabilité : Point d’éclair à 40 °C, ce qui le rend inflammable dans certaines conditions.
- Corrosivité : Peut attaquer certains métaux comme le zinc et le fer, en formant des acétates métalliques et en libérant du dihydrogène.
L’acide acétique forme des dimères moléculaires en phase gazeuse et en solution non aqueuse. Ces structures sont stabilisées par des liaisons hydrogène entre les groupes carboxyle des molécules, ce qui modifie certaines de ses propriétés physico-chimiques.
Histoire et découverte
L’utilisation de l’acide acétique remonte à l’Antiquité, où il était principalement consommé sous forme de vinaigre. Les premières mentions de sa production datent de plusieurs millénaires, avec la fermentation naturelle des boissons alcoolisées laissées à l’air libre.
- Antiquité :
- Les Égyptiens et les Babyloniens utilisaient le vinaigre pour la conservation des aliments.
- Théophraste, philosophe grec du IIIᵉ siècle av. J.-C., décrit l’effet du vinaigre sur les métaux et sa transformation en sels d’acétate.
- Moyen Âge et Renaissance :
- Les alchimistes améliorent la distillation du vinaigre pour obtenir des concentrations plus élevées d’acide acétique.
- L’acide acétique glacial est produit par distillation sèche d’acétates métalliques (notamment l’acétate de plomb).
- XIXᵉ et XXᵉ siècles :
- En 1847, Hermann Kolbe réussit à synthétiser l’acide acétique à partir de composés inorganiques, ouvrant la voie à la production industrielle.
- Vers 1910, la production d’acide acétique repose principalement sur la distillation du bois (liqueur pyroligneuse).
- Vers 1910, la production d’acide acétique repose principalement sur la distillation du bois (liqueur pyroligneuse).
Aujourd’hui, plus de 6,5 millions de tonnes d’acide acétique sont produites chaque année dans le monde, avec une demande croissante dans les secteurs chimique, pharmaceutique et alimentaire.

Production et synthèse de l’acide acétique
L’acide acétique est produit à l’échelle industrielle par divers procédés, permettant d’obtenir une pureté adaptée aux besoins des différentes applications. Bien que la production par fermentation bactérienne soit historiquement la plus ancienne, elle est aujourd’hui marginale au profit de procédés chimiques modernes, plus efficaces et adaptés aux exigences industrielles.
Méthodes industrielles de fabrication
Carbonylation du méthanol : procédé dominant
La méthode la plus couramment utilisée pour la production industrielle de l’acide acétique est la carbonylation du méthanol, qui représente environ 75 % de la production mondiale. Ce procédé repose sur la réaction du méthanol (CH₃OH) avec du monoxyde de carbone (CO) sous catalyse homogène.
Réaction chimique :
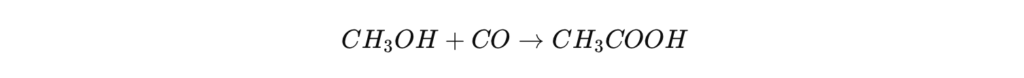
Le procédé Monsanto, développé dans les années 1970 par l’entreprise Monsanto, utilise le rhodium (Rh) comme catalyseur principal. Il a été remplacé dans les années 1990 par le procédé Cativa, mis au point par BP Chemicals, qui repose sur un catalyseur à base d’iridium (Ir), plus efficace et générant moins de sous-produits indésirables.
Avantages de la carbonylation du méthanol :
- Haut rendement (supérieur à 95 %).
- Moins de déchets et de sous-produits polluants.
- Réduction des coûts de production grâce aux catalyseurs optimisés.
Oxydation de l’acétaldéhyde
Avant la généralisation du procédé Monsanto, la principale méthode de production de l’acide acétique reposait sur l’oxydation de l’acétaldéhyde (CH₃CHO) à l’aide de l’oxygène de l’air sous l’effet d’un catalyseur métallique (manganèse, cobalt ou chrome).
Réaction chimique :
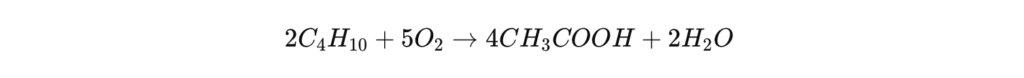
Bien que toujours utilisée, cette méthode est désormais minoritaire en raison de son rendement inférieur à 85 % et de la présence de sous-produits secondaires tels que l’acide formique et l’acétate d’éthyle.
Oxydation du butane et de l’éthylène
Une autre alternative industrielle consiste à oxyder du butane (C₄H₁₀) ou de l’éthylène (C₂H₄) en phase liquide, en présence d’un catalyseur métallique.
Réaction chimique pour le butane :
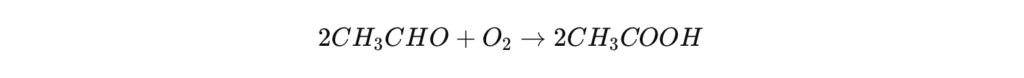
Ce procédé, utilisé par certaines industries, permet d’obtenir de l’acide acétique de haute pureté, mais il est moins rentable que la carbonylation du méthanol, en raison de son coût énergétique plus élevé.
Fermentation bactérienne : une production naturelle
La production d’acide acétique par fermentation bactérienne est principalement utilisée pour la fabrication de vinaigre, notamment pour des applications alimentaires. Ce procédé repose sur l’action des bactéries acétiques du genre Acetobacter, qui transforment l’éthanol (C₂H₅OH) en acide acétique en présence d’oxygène.
Réaction biologique :
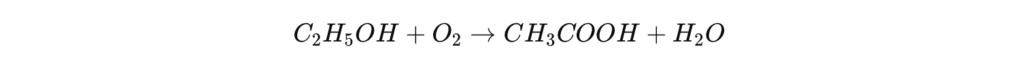
Ce procédé est peu efficace pour une production industrielle de grande envergure, mais il reste indispensable pour la production de vinaigre, car la réglementation impose que le vinaigre destiné à la consommation humaine soit issu d’un processus biologique.
Principaux producteurs et marché mondial
Production mondiale et répartition géographique
La production mondiale d’acide acétique est estimée à environ 6,5 millions de tonnes par an. Elle est concentrée dans quelques pays industrialisés disposant de grandes capacités pétrochimiques.
- États-Unis : premier producteur mondial, avec une capacité annuelle supérieure à 2,5 millions de tonnes.
- Chine : production en forte croissance, notamment grâce aux investissements dans la pétrochimie.
- Europe : production en baisse, avec une capacité d’environ 1 million de tonnes par an.
- Japon : acteur historique du marché, produisant environ 0,7 million de tonnes.
Acteurs majeurs de l’industrie
Quelques entreprises dominent la production mondiale d’acide acétique, notamment :
- Celanese (États-Unis)
- BP Chemicals (Royaume-Uni)
- Eastman Chemical Company (États-Unis)
- LyondellBasell (Pays-Bas)
- Daicel (Japon)
Ces entreprises contrôlent la production et l’approvisionnement mondial, influençant directement les prix et la disponibilité de l’acide acétique sur le marché.
Enjeux économiques et environnementaux
L’acide acétique est un intermédiaire clé dans l’industrie chimique, utilisé dans la fabrication de plastiques, solvants et produits pharmaceutiques. Cependant, son impact environnemental est surveillé en raison de la production de CO₂ et de composés volatils lors de certains procédés.
Les défis actuels du secteur incluent :
- Optimisation des procédés pour limiter les émissions de gaz à effet de serre.
- Recyclage des flux secondaires pour réduire les déchets industriels.
- Développement de catalyseurs plus performants pour augmenter les rendements et limiter les sous-produits.
L’évolution des réglementations internationales impose aux industriels de réduire l’impact environnemental des procédés chimiques, ce qui pourrait encourager le développement de nouvelles techniques de production plus écologiques.
Vous recherchez une analyse ?

Utilisations et applications de l’acide acétique
L’acide acétique est un composé polyvalent utilisé dans de nombreux secteurs industriels. Son rôle s’étend de l’industrie chimique à l’agroalimentaire en passant par la pharmacie, les plastiques et les textiles. Grâce à ses propriétés acides et solvantées, il intervient dans la fabrication de produits aussi variés que les polymères, les solvants, les additifs alimentaires et les médicaments.
Industrie chimique et pharmaceutique
Fabrication de l’anhydride acétique et des acétates
L’acide acétique est un précurseur essentiel dans la production de l’anhydride acétique (C₄H₆O₃), une substance réactive utilisée dans la synthèse de nombreux composés organiques. Il est principalement employé pour :
- La fabrication de l’acétate de cellulose, utilisé dans la production de films plastiques, de textiles synthétiques et de filtres à cigarettes.
- La synthèse de l’acide acétylsalicylique (aspirine), qui repose sur une réaction entre l’anhydride acétique et l’acide salicylique.
L’anhydride acétique est aussi utilisé dans la fabrication d’héroïne, ce qui en fait un produit strictement contrôlé par les autorités réglementaires.
Production de solvants et plastiques
L’acide acétique est un intermédiaire clé dans la fabrication de l’acétate de vinyle monomère (VAM), un composé essentiel pour la production de polymères et de résines. Il intervient notamment dans la fabrication de :
- Peintures et adhésifs, via le polyacétate de vinyle (PVA).
- Films plastiques et fibres textiles, par la polymérisation de l’acétate de vinyle.
D’autres solvants industriels, comme l’acétate d’éthyle et l’acétate de butyle, sont produits à partir de l’acide acétique et sont utilisés dans l’industrie des peintures, des vernis et des encres d’impression.
Utilisation pharmaceutique et désinfectante
L’acide acétique est employé dans l’industrie pharmaceutique pour ses propriétés antiseptiques et bactériostatiques. Il est notamment utilisé pour :
- Désinfecter les plaies et les surfaces médicales sous forme de solutions diluées.
- Traiter certaines infections bactériennes en dermatologie et en otorhinolaryngologie.
- Servir d’excipient dans des formulations pharmaceutiques, en tant qu’ajusteur de pH.
Agroalimentaire : rôle et réglementation
L’acide acétique en tant qu’additif alimentaire (E260)
L’acide acétique est un régulateur d’acidité largement utilisé dans l’industrie alimentaire sous le code E260. Il est présent dans :
- Les vinaigres alimentaires, dont il est le principal constituant actif.
- Les sauces, marinades et condiments, où il renforce la saveur et la conservation.
- Les produits de boulangerie, pour contrôler l’acidité et la fermentation.
L’Union européenne et la Food and Drug Administration (FDA) autorisent l’utilisation de l’acide acétique dans l’alimentation sous certaines limites strictes de concentration.
Production de vinaigre par fermentation
Le vinaigre est une solution aqueuse d’acide acétique obtenue par fermentation biologique de l’éthanol en présence de bactéries du genre Acetobacter. Ce processus naturel est utilisé depuis des millénaires pour la conservation des aliments.
Types de vinaigres selon leur origine :
- Vinaigre de vin : issu de la fermentation du vin rouge ou blanc.
- Vinaigre de cidre : produit à partir de pommes fermentées.
- Vinaigre balsamique : fabriqué à partir de moût de raisin concentré et vieilli en fût de bois.
Le vinaigre alimentaire doit contenir au moins 4 % d’acide acétique pour être commercialisé en Europe.
Réglementation et sécurité alimentaire
L’utilisation de l’acide acétique dans l’agroalimentaire est strictement réglementée pour garantir la sécurité des consommateurs. Les principaux cadres réglementaires sont :
- Le règlement CE n° 1333/2008 de l’Union européenne, qui définit les conditions d’utilisation des additifs alimentaires.
- Les normes de pureté imposées par le Codex Alimentarius.
- Les contrôles de migration dans les emballages alimentaires, en conformité avec le règlement CE n° 1935/2004.
Autres applications industrielles
Industrie textile et tannerie
L’acide acétique est utilisé dans l’industrie textile pour :
- Fixer les colorants sur les fibres naturelles et synthétiques, en ajustant le pH des bains de teinture.
- Améliorer la tenue des impressions sur tissus, notamment pour les textiles en coton et polyester.
Dans la tannerie, il est utilisé pour le prétraitement des peaux (piclage) avant le tannage, en ajustant leur pH pour optimiser l’absorption des agents tannants.
Photographie et électronique
Dans les procédés de développement photographique, l’acide acétique est utilisé sous forme de bain d’arrêt pour interrompre l’action du révélateur et fixer l’image.
Dans l’industrie électronique, il intervient comme agent de nettoyage dans la fabrication des semi-conducteurs, notamment pour éliminer les résidus métalliques et ajuster les surfaces des composants électroniques.
Nettoyage et désinfection
L’acide acétique dilué est un agent de détartrage et de nettoyage efficace pour :
- Éliminer les dépôts de calcaire et de tartre dans les machines et installations industrielles.
- Désinfecter les surfaces et les équipements dans les secteurs agroalimentaire et médical.
Son action contre les bactéries et les moisissures en fait un ingrédient clé dans certains produits de nettoyage écologiques, notamment les nettoyants multi-usages à base de vinaigre.
L’acide acétique joue donc un rôle essentiel dans de nombreuses applications industrielles, en raison de ses propriétés chimiques spécifiques et de sa large disponibilité sur le marché mondial.

Analyses de laboratoire sur l’acide acétique
L’acide acétique est largement utilisé dans l’industrie, ce qui impose des analyses rigoureuses pour garantir sa pureté, sa conformité réglementaire et sa sécurité dans les différentes applications. Les laboratoires spécialisés réalisent des tests pour vérifier la concentration de l’acide acétique, détecter les impuretés et s’assurer que les produits contenant cette substance répondent aux exigences normatives.
Importance des analyses et enjeux réglementaires
Les contrôles en laboratoire sont essentiels pour :
- Garantir la qualité et la pureté de l’acide acétique utilisé dans l’industrie chimique, pharmaceutique et alimentaire.
- Vérifier la conformité réglementaire selon les normes ISO 17025 et les accréditations COFRAC.
- Détecter les impuretés et contaminants, notamment les traces de métaux lourds, de solvants résiduels et de sous-produits de synthèse.
- Évaluer la concentration en acide acétique dans divers produits, tels que le vinaigre, les solvants et les solutions industrielles.
Dans le cadre de la production alimentaire et pharmaceutique, les laboratoires doivent respecter des réglementations strictes, notamment :
- Règlement CE n° 1333/2008 pour les additifs alimentaires.
- Règlement CE n° 1935/2004 sur les matériaux en contact avec les aliments.
- Normes de pharmacopée européenne pour les produits pharmaceutiques.
Techniques d’analyse utilisées
Différentes méthodes analytiques permettent de mesurer la concentration d’acide acétique et d’identifier ses impuretés dans diverses matrices.
Chromatographie liquide haute performance (HPLC)
La HPLC est une technique couramment utilisée pour l’analyse de l’acide acétique dans les produits agroalimentaires, pharmaceutiques et chimiques. Elle permet de :
- Quantifier précisément la teneur en acide acétique.
- Séparer et identifier les impuretés présentes dans un échantillon.
- Vérifier la conformité du produit aux normes en vigueur.
Elle est particulièrement utilisée pour le contrôle qualité du vinaigre, où elle permet de déterminer la concentration exacte en acide acétique et de s’assurer qu’elle respecte la réglementation.
Chromatographie ionique
La chromatographie ionique est employée pour détecter et mesurer les acides volatils, y compris l’acide acétique, dans l’air, l’eau et les matériaux. Cette technique est essentielle pour :
- Contrôler la pollution industrielle et environnementale.
- Vérifier la concentration d’acide acétique dans les solvants et solutions aqueuses.
Spectroscopie infrarouge à transformée de Fourier (FTIR)
La FTIR permet d’identifier l’acide acétique grâce à ses liaisons spécifiques C=O et O-H. Cette méthode est utilisée pour :
- Déterminer la structure chimique et la pureté du produit.
- Vérifier la présence d’impuretés dans les formulations chimiques.
Titration acide-base
Le titrage acide-base est une méthode classique permettant de mesurer la concentration d’acide acétique dans une solution. Elle repose sur la neutralisation de l’acide par une base forte (NaOH), avec utilisation d’un indicateur de pH. Cette technique est :
- Simple et rapide, adaptée aux analyses courantes.
- Précise pour des solutions aqueuses, comme les vinaigres ou les solutions d’acide acétique dilué.
Chromatographie en phase gazeuse couplée à la spectrométrie de masse (GC-MS)
La GC-MS est utilisée pour l’analyse de l’acide acétique dans l’eau et les matrices complexes. Cette méthode est essentielle pour :
- Détecter la présence d’acide acétique dans des mélanges volatils.
- Identifier les contaminants associés à sa production.
Tests de migration pour les matériaux en contact avec des aliments
L’acide acétique étant un agent de régulation du pH, il est souvent utilisé dans les emballages alimentaires pour tester la migration des substances chimiques.
Réglementation et importance des tests de migration
Les emballages plastiques, papiers, encres et vernis doivent être conformes au règlement CE n° 1935/2004, qui impose des limites strictes sur la migration des composés chimiques vers les aliments.
Les tests de migration réalisés en laboratoire permettent de :
- Évaluer l’interaction entre l’emballage et les aliments contenant de l’acide acétique.
- Vérifier que les matériaux ne libèrent pas de substances toxiques sous l’effet de l’acidité.
- Garantir la conformité des emballages aux normes européennes et américaines (FDA).
Méthodes de test en laboratoire
Les laboratoires simulent des conditions réelles d’utilisation en mettant en contact l’emballage avec une solution d’acide acétique à 3 % ou 10 %, puis mesurent la migration des substances à l’aide de :
- Chromatographie liquide haute performance (HPLC) pour détecter les contaminants.
- Spectrométrie de masse (GC-MS ou ICP-MS) pour l’identification des composés migrés.
Analyses rhéologiques et impact sur les formulations
L’acide acétique influence la texture et la stabilité des formulations industrielles, notamment dans les produits agroalimentaires et cosmétiques.
Étude de la viscosité et de la fluidité
Les laboratoires réalisent des tests rhéologiques pour analyser :
- La fluidité et la texture des sauces, crèmes et produits alimentaires, où l’acide acétique peut jouer un rôle stabilisant.
- La viscosité des solutions pharmaceutiques et cosmétiques, où il intervient dans la régulation du pH.
Ces analyses sont effectuées à l’aide de rhéomètres, permettant de mesurer la réponse du produit sous l’effet de contraintes mécaniques.
Stabilité et compatibilité des formulations
L’ajout d’acide acétique dans une formulation peut affecter :
- La stabilité des émulsions et crèmes, nécessitant un ajustement du pH.
- L’interaction avec d’autres ingrédients, en particulier les polymères et les agents épaississants.
Les tests réalisés en laboratoire permettent d’optimiser les formulations pour garantir une meilleure conservation et un comportement optimal du produit.
L’analyse de l’acide acétique en laboratoire est donc essentielle pour assurer sa qualité, sa conformité réglementaire et son intégration dans diverses applications industrielles.
Risques et précautions liés à l’acide acétique
L’acide acétique, bien qu’utilisé dans de nombreuses applications industrielles et alimentaires, présente certains risques pour la santé et l’environnement. Il est important de connaître ses effets, ses dangers et les précautions nécessaires pour une manipulation sécurisée.
Toxicité et effets sur la santé
L’acide acétique peut avoir des effets nocifs en fonction de sa concentration et de son mode d’exposition.
Exposition par inhalation
Les vapeurs d’acide acétique sont irritantes pour les voies respiratoires et peuvent provoquer :
- Des toux et irritations à partir d’une exposition prolongée.
- Une sensation de brûlure dans le nez et la gorge, même à faible concentration.
- Des œdèmes pulmonaires en cas d’exposition à des concentrations élevées (supérieures à 25 ppm).
Contact avec la peau et les yeux
L’acide acétique est corrosif à haute concentration et peut entraîner :
- Des brûlures cutanées graves en cas de contact avec l’acide acétique glacial.
- Une irritation sévère des yeux, pouvant provoquer une conjonctivite chimique.
- Des lésions tissulaires irréversibles, en cas d’exposition prolongée à des solutions concentrées.
Effets d’une ingestion accidentelle
L’ingestion d’acide acétique hautement concentré peut être très dangereuse :
- Brûlures de l’œsophage et de l’estomac.
- Douleurs abdominales et vomissements.
- Risque de perforation gastrique en cas d’exposition à de fortes concentrations.
Les solutions diluées, comme le vinaigre alimentaire, ne présentent pas de risque significatif pour la santé aux doses usuelles de consommation.
Réglementation sur l’exposition professionnelle
L’acide acétique est soumis à des limites d’exposition en milieu professionnel pour protéger les travailleurs.
Valeurs limites d’exposition (VLE)
Les réglementations fixent des valeurs limites d’exposition pour éviter les risques sanitaires :
- VLE en France (INRS) :
- 10 ppm (25 mg/m³) sur 8 heures.
- 15 ppm (37 mg/m³) en exposition courte (15 minutes).
- Normes OSHA (États-Unis) : 10 ppm sur 8 heures.
Classification de danger selon le règlement CLP
L’acide acétique est classé comme substance dangereuse selon le règlement CE n° 1272/2008 (CLP) :
- H226 : Liquide et vapeurs inflammables.
- H314 : Provoque des brûlures de la peau et des lésions oculaires graves.
- H335 : Peut irriter les voies respiratoires.
Les entreprises manipulant l’acide acétique doivent mettre en place des mesures de prévention adaptées pour éviter toute exposition dangereuse.
Mesures de sécurité et stockage
Une manipulation sécurisée de l’acide acétique est essentielle pour réduire les risques d’accident.
Équipements de protection individuelle (EPI)
es travailleurs exposés doivent porter :
- Des gants résistants aux produits chimiques, en nitrile ou néoprène.
- Des lunettes de protection ou un écran facial.
- Un masque avec filtre adapté aux vapeurs acides, en cas d’utilisation prolongée.
- Une combinaison de protection, pour éviter tout contact avec la peau.
Conditions de stockage
L’acide acétique doit être stocké avec précaution pour éviter les risques d’incendie et de réaction chimique.
- Stocker dans un endroit ventilé et frais, loin des sources de chaleur.
- Utiliser des récipients résistants à la corrosion, comme l’acier inoxydable ou le plastique haute densité.
- Éviter tout contact avec des bases fortes, des oxydants puissants ou des métaux réactifs, qui pourraient provoquer des réactions dangereuses.
Procédures en cas de fuite ou d’accident
En cas de déversement accidentel, il est recommandé de :
- Évacuer la zone et limiter l’exposition aux vapeurs.
- Neutraliser la fuite avec du bicarbonate de sodium avant de nettoyer.
- Éliminer les déchets conformément aux réglementations environnementales.
Impact environnemental et élimination des déchets
L’acide acétique, bien que biodégradable, peut avoir un impact environnemental s’il est rejeté en grande quantité.
Effets sur l’environnement
- Contamination des eaux : un rejet excessif peut acidifier les milieux aquatiques, mettant en danger la faune et la flore.
- Émissions atmosphériques : les vapeurs peuvent contribuer à l’irritation de l’air en milieu urbain ou industriel.
Élimination des déchets industriels
Les entreprises utilisant de l’acide acétique doivent suivre des protocoles stricts pour l’élimination des déchets :
- Neutralisation avant rejet : il est souvent neutralisé avec une base comme l’hydroxyde de sodium (NaOH) avant d’être rejeté dans les eaux usées.
- Traitement par incinération contrôlée pour éviter la dispersion dans l’environnement.
- Respect des normes européennes et locales pour le traitement des déchets chimiques.
L’acide acétique, bien que couramment utilisé, nécessite donc une manipulation rigoureuse, des protocoles de sécurité adaptés et une gestion contrôlée des déchets pour limiter ses risques pour la santé et l’environnement.
YesWeLab : des solutions d’analyse pour l’acide acétique
L’analyse de l’acide acétique est essentielle pour garantir la qualité, la conformité réglementaire et la sécurité des produits qui en contiennent. YesWeLab, grâce à son réseau de plus de 200 laboratoires partenaires, propose des solutions analytiques adaptées aux besoins des industriels de divers secteurs.
Pourquoi analyser l’acide acétique avec YesWeLab ?
Les industriels utilisant de l’acide acétique dans leurs formulations doivent réaliser des analyses précises et conformes aux normes en vigueur. YesWeLab offre des prestations analytiques permettant de :
- Contrôler la pureté et la concentration de l’acide acétique dans les matières premières et produits finis.
- Détecter les impuretés et contaminants, comme les solvants résiduels ou les métaux lourds.
- Garantir la sécurité des consommateurs et des travailleurs en évaluant les éventuels risques liés à son utilisation.
Grâce à son expertise, YesWeLab accompagne les entreprises dans leurs démarches de certification et de validation de produits contenant de l’acide acétique.
Processus d’analyse avec YesWeLab
YesWeLab facilite l’accès aux analyses de laboratoire grâce à un processus simplifié et digitalisé.
Les industriels peuvent trouver les analyses adaptées à leurs besoins en consultant le catalogue en ligne de YesWeLab, qui propose plus de 10 000 prestations analytiques.
Parmi les analyses disponibles pour l’acide acétique :
- Dosage de l’acide acétique dans les solvants, produits alimentaires et pharmaceutiques.
- Recherche d’impuretés et de solvants résiduels.
- Tests de migration pour les emballages en contact avec des produits acides.
- Analyses de stabilité et compatibilité des formulations.
Analyse en laboratoire
Les échantillons sont pris en charge par des laboratoires, équipés des dernières technologies analytiques :
- Chromatographie liquide haute performance (HPLC).
- Chromatographie ionique.
- Spectroscopie FTIR.
- Titration acide-base.
- GC-MS pour les solvants et matrices complexes.
Tests spécifiques pour les matériaux en contact avec l’acide acétique
YesWeLab propose des tests de migration pour s’assurer que les emballages et matériaux respectent les normes en vigueur. Ces tests sont particulièrement importants pour :
- Les emballages alimentaires, afin d’éviter la contamination des produits acides.
- Les revêtements et plastiques industriels, pour garantir leur résistance à l’acidité.
- Les équipements de production, afin de prévenir la corrosion et l’usure des matériaux.
L’acide acétique étant largement utilisé dans de nombreux secteurs, il est essentiel de garantir sa qualité et sa conformité à travers des analyses rigoureuses. En faisant appel à YesWeLab, les industriels bénéficient d’un service complet et digitalisé, leur permettant d’optimiser leurs formulations et de garantir la sécurité de leurs produits.



